간세포암은 전 세계적으로 가장 흔한 원발성 간암이며(원발성 간암의 70%~90%를 차지합니다), 암 관련 사망의 주요 원인 중 하나입니다. 간세포 손상 후 간암이 발생하는 것은 분자유전적 변화와 미세환경 이상이 수반되는 다단계, 다인자에 의해 구동되는 복잡한 병리학적 과정이며, 핵심 논리는 "지속적 손상→비정상적 복구→세포 악성화→종양 진행"의 악순환입니다. 이 과정은 보통 수년에서 수십년이 걸리며, 손상 메커니즘은 유발인자(예: B형 간염 바이러스, 알코올, 비알코올성 지방간 질환 등)가 다르면 미세하게 다르지만 최종 경로에는 공통점이 있습니다[1].
바이러스 감염(HBV/HCV, 주요 유발인자);
알코올성 간손상;
비알코올성 지방간 질환(NAFLD/NASH);
화학적 발암물질(예: 아플라톡신 B1, AFB1)[2].
간세포가 괴사/세포자살한 후 간은 "간세포 증식 인자(HGF)"를 방출하여 남아있는 간세포의 증식(재생)을 자극하지만, 증식이 너무 빠르면 DNA 복제 오류 확률이 높아집니다("복제가 많을수록 돌연변이 위험이 높다"와 동일합니다);
간성상세포(HSC)는 염증성 인자에 의해 활성화되어 "근섬유아세포"로 변환되고 다량의 콜라겐을 분비하여 간섬유화를 형성합니다. 섬유화는 간의 구조적 변형을 유발할 뿐만 아니라 "저산소 미세환경"(콜라겐 섬유가 혈관을 압박하여 혈류를 감소시킵니다)을 형성하며, 저산소는 "저산소 유도 인자(HIF-1α)"를 활성화시켜 이후 종양 혈관 신생을 촉진합니다(암으로 가는 길을 열어줍니다).
염증세포(대식세포, T세포)는 지속적으로 침윤하고, 방출된 염증성 인자(IL-6 등)는 "JAK-STAT3 경로"를 통해 간세포의 생존과 증식을 촉진합니다. 세포에 이미 DNA 손상이 있더라도 세포자살로 제거되지 않고 "강제로 유지"됩니다(이것이 "염증성 암"의 핵심 메커니즘입니다)[3,4].
p53: 가장 흔하게 불활성화되는 종양 억제 유전자입니다(약 50%의 HCC에서 p53 변이가 존재합니다). 불활성화 후 손상된 세포의 분열을 방지할 수 없고 비정상 세포자살을 유도할 수 없기 때문에 변이 세포의 "무제한 생존"을 유발합니다;
p16INK4a: 메틸화 또는 결실로 인해 불활성화되어 "사이클린 의존성 키나아제(CDK4/6)"를 억제할 수 없게 되어 세포 주기 상실(DNA 복구 체크포인트를 건너뛰고 G1기에서 S기로 직접 이동)을 유발합니다;
PTEN: 포스파테이즈 유전자입니다. 불활성화 후 "PI3K-Akt 경로"를 억제할 수 없게 되어, 이 경로의 지속적 활성화는 세포 증식을 촉진하고 세포자살을 억제하며 세포 침윤을 강화합니다.
Ras 패밀리(K-Ras, H-Ras): 변이 후 "Ras-MAPK 경로"의 지속적 활성화는 세포 증식의 핵심 신호이며, 간세포에 무제한으로 분열하도록 "강제"합니다;
β-카테닌: Wnt 신호 전달 경로의 핵심 분자입니다. 변이 후 세포 내에 축적되고 핵으로 들어간 후 전사 인자와 결합하여 "사이클린 D1 및 c-Myc" 등 증식 관련 유전자의 발현을 촉진하고 세포 분화를 억제합니다(세포를 "미성숙한" 증식 상태로 유지합니다);
MET: HGF의 수용체 유전자입니다. 증폭 또는 변이 후 지속적으로 활성화되어 간세포의 증식과 이동을 촉진합니다(이후 전이로 가는 길을 열어줍니다)[5,6].
혈관 신생 시작: 저산소 미세환경에 의해 활성화된 저산소 유도 인자(HIF-1α)는 혈관 내피 성장 인자(VEGF)의 발현을 촉진합니다. 이로 인해 내피 세포가 종양 조직으로 이동하여 "비정상 종양 혈관"을 형성합니다 - 이것은 암의 중요한 마커입니다. 왜냐하면 종양 세포는 영양 공급을 위해 혈관이 필요하며 "밀리미터 크기 결절"에서 "센티미터 크기 종양"으로 성장하기 때문입니다;
면역 회피: 종양 세포는 여러 방법으로 면역계의 제거를 회피합니다:
"PD-L1" 분자를 발현하여 면역 세포(T세포)의 PD-1에 결합하여 T세포의 활성을 억제합니다;
"형질전환 성장 인자 β(TGF-β)"를 분비하여 조절성 T세포(Treg)의 응집을 유도하고 면역 반응을 억제합니다;
"주요 조직 적합 복합체(MHC)"의 발현을 낮추어 면역 세포가 종양 세포를 인식할 수 없도록 만듭니다[7].
면역 회피: 종양 세포는 여러 방법으로 면역계의 제거를 회피합니다:
"PD-L1" 분자를 발현하여 면역 세포(T세포)의 PD-1에 결합하여 T세포의 활성을 억제합니다;
"형질전환 성장 인자 β(TGF-β)"를 분비하여 조절성 T세포(Treg)의 응집을 유도하고 면역 반응을 억제합니다;
"주요 조직 적합 복합체(MHC)"의 발현을 낮추어 면역 세포가 종양 세포를 인식할 수 없도록 만듭니다[7].
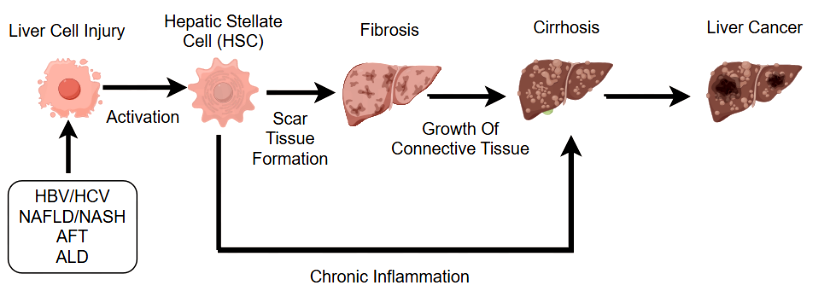
간세포암 메커니즘 도해
| Target | Catalog# | Product Name | Reactivity | Application |
|---|---|---|---|---|
| Antibodies related to the uncontrolled proliferation pathway of hepatic stellate cells: | ||||
| KRAS | APRab13128 | K-Ras Rabbit Polyclonal Antibody | Human,Mouse,Rat | WB,IHC-P,IF-P,IF-F,ICC/IF,ELISA |
| B-Raf | APRab07417 | BACE Rabbit Polyclonal Antibody | Human,Mouse,Rat | IHC-P,IF-P,IF-F,ICC/IF,ELISA |
| MEK1 | AMRe04007 | MEK1 Rabbit Monoclonal Antibody | Human,Mouse,Rat | WB,IHC-F,IHC-P,ICC/IF,FC |
| MEK1 |
| |||
