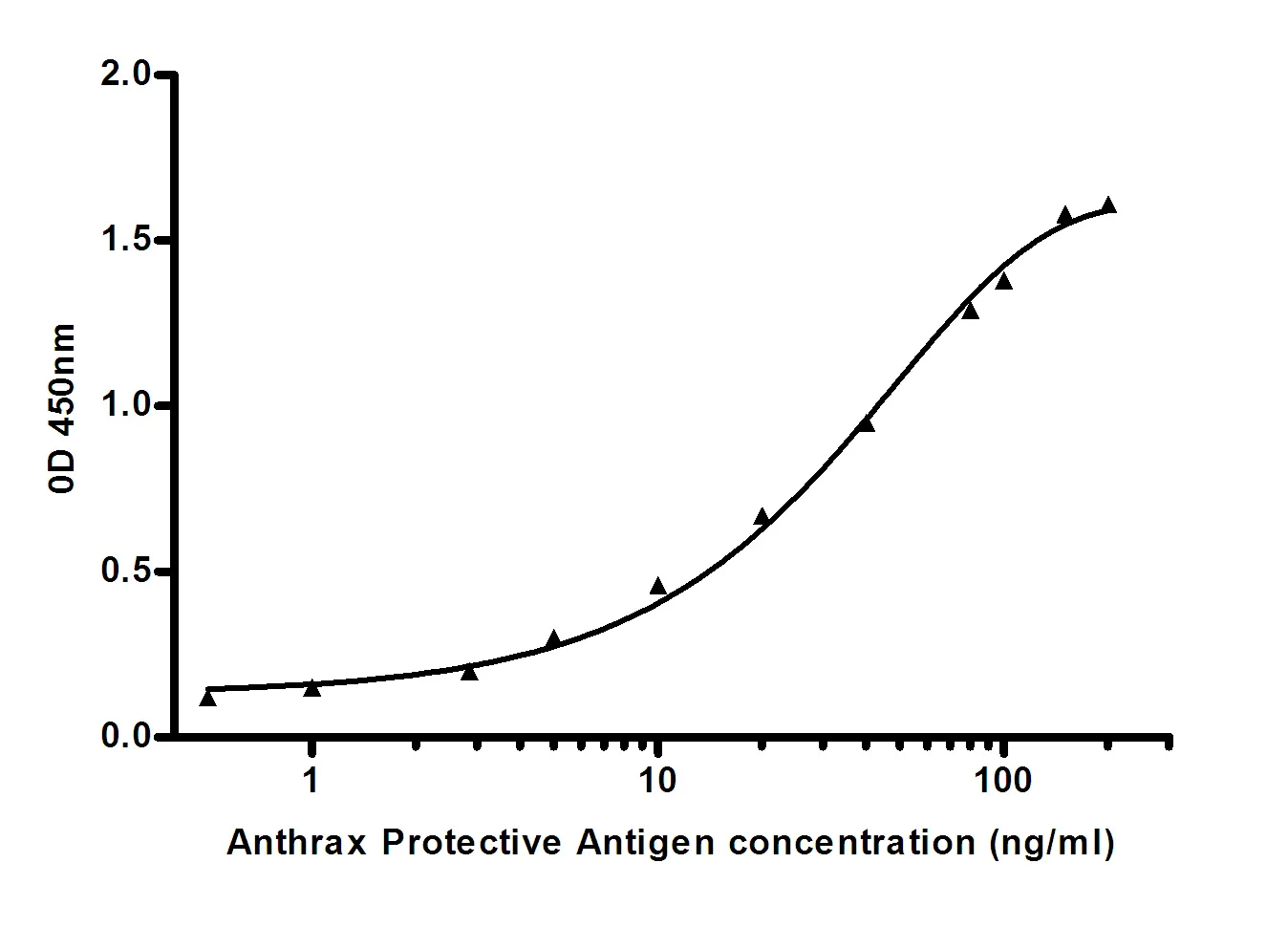
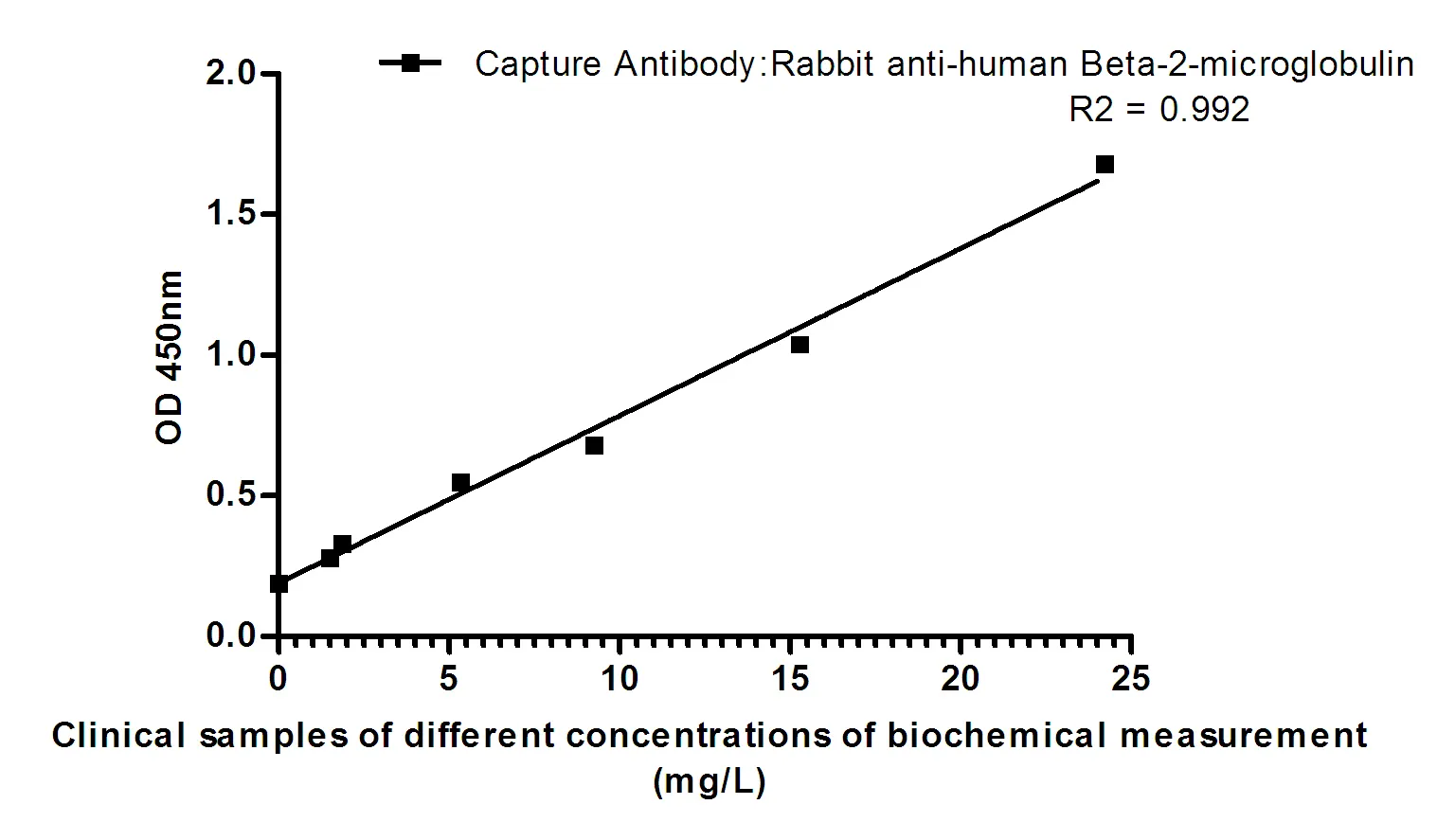
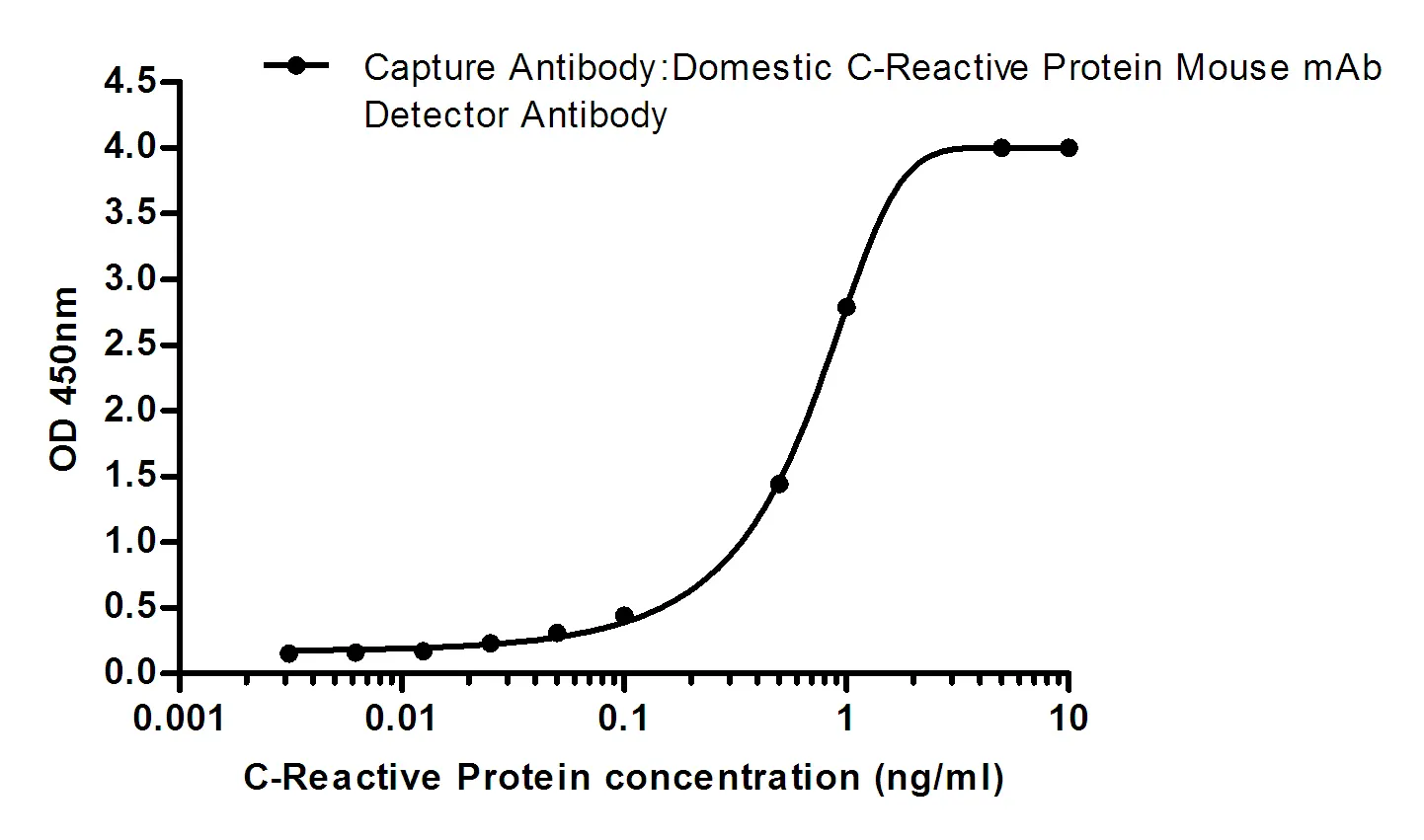
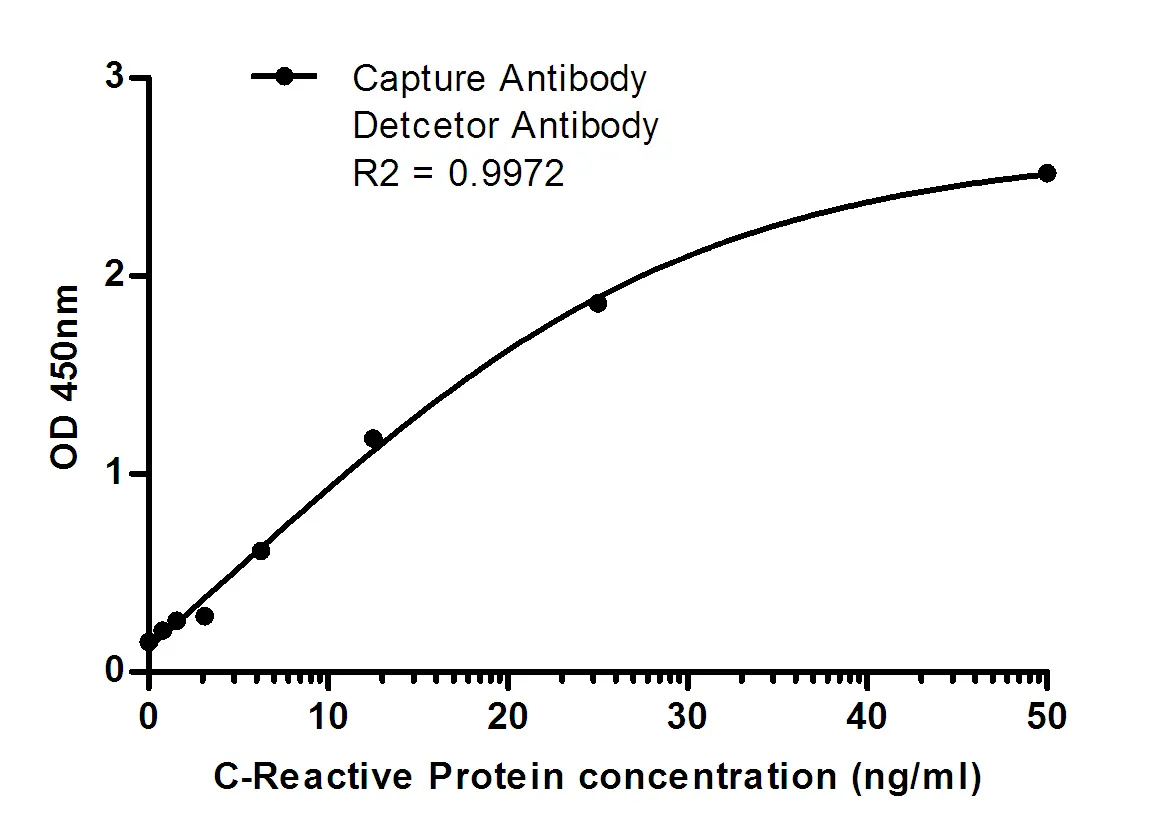
TTR(1D7)마우스 단클론 항체
접합: 비결합
마우스 단클론 항체
응용 분야
반응성
인간
유전자 이름
TTR PALB
저장
소분하여 -20°C에서 보관하십시오(유통기한 12개월). 냉동/해동 과정을 반복하지 마십시오.
요약
| 제품 이름 | TTR(1D7)마우스 단클론 항체 |
| 설명 | 마우스 단클론 항체 |
| 숙주 | 생쥐 |
| 반응성 | 인간 |
| 접합 | 비결합 |
| 변형 | 수정되지 않음 |
| 동형 | IgG |
| 클론성 | 단클론 |
| 형태 | 액체 |
| 농도 | 비결합 |
| 저장 | 소분하여 -20°C에서 보관하십시오(유통기한 12개월). 냉동/해동 과정을 반복하지 마십시오. |
| 배송 | 얼음주머니. |
| 완충액 | 글리세롤 50%, 보호 단백질 0.5%, 신규 방부제 N 0.02%를 함유한 PBS 용액. |
| 정제 | 친화성 정제 |
항원 정보
| 유전자 이름 | TTR PALB |
| 대체 이름 | Transthyretin (ATTR) (Prealbumin) (TBPA) |
| Gene ID | 7276 |
| SwissProt ID | P02766 |
| Immunogen | TTR의 재조합 단백질 |
응용 분야
| 응용 분야 | WB,IHC,ICC/IF |
| 희석 비율 | WB 1:500-1:2000,IHC 1:50-1:300,ICC/IF 1:50-1:200 |
| 분자량 | 16kDa |
연구 분야
| Neuroscience |
배경
| 이 유전자는 알파-1-안티트립신, 트랜스티레틴, 오로소무코이드와 함께 세 가지 프리알부민 중 하나인 트랜스티레틴을 코딩합니다. 트랜스티레틴은 운반 단백질로, 혈장과 뇌척수액에서 갑상선 호르몬을 운반하고 혈장에서 레티놀(비타민 A)도 운반합니다. 이 단백질은 동일한 소단위체 4개가 결합된 사량체 구조입니다. 이 유전자에서는 80가지가 넘는 다양한 돌연변이가 보고되었으며, 대부분은 아밀로이드 침착과 관련되어 주로 말초 신경 및/또는 심장에 영향을 미칩니다. 소수의 돌연변이는 아밀로이드 침착과 관련이 없습니다. 돌연변이로 인해 발생하는 질환에는 아밀로이드성 다발신경병증, 정상 갑상선 기능 항진증, 아밀로이드성 유리체 혼탁, 심근병증, 안구수막 아밀로이드증, 수막뇌혈관 아밀로이드증, 수근관 증후군 등이 있습니다. [RefSeq 제공, 2009년 1월], 질환: TTR 결함은 갑상선 기능 항진증의 원인입니다 [MIM:176300]. 질환: TTR 결함은 1형 아밀로이드증(AMYL1)의 원인입니다 [MIM:176300]. AMYL1은 트랜스티레틴 아밀로이드 침착으로 인한 유전성 전신 아밀로이드증입니다. 단백질 섬유는 다양한 조직에서 형성되어 아밀로이드성 다발신경병증, 아밀로이드성 심근병증, 수근관 증후군, 전신성 노인성 아밀로이드증을 유발할 수 있습니다. 질환: 트랜스티레틴(TTR) 결함은 7형 아밀로이드증(AMYL7)[MIM:105210]의 원인이며, 연수막 아밀로이드증 또는 뇌수막혈관 아밀로이드증으로도 알려져 있습니다. AMYL7은 중추신경계를 주로 침범하는 유전성 트랜스티레틴 아밀로이드증의 한 형태입니다. 신경병리학적 검사에서 연수막 혈관벽, 연막, 지주막, 그리고 연막하 침착물에서 아밀로이드가 관찰됩니다. 일부 환자에서는 시력 장애를 유발하는 유리체 아밀로이드 침착(안구연수막 아밀로이드증)도 발생합니다. 임상적 특징으로는 발작, 뇌졸중 유사 증상, 치매, 정신운동 기능 저하, 유리체 내 다양한 정도의 아밀로이드 침착 등이 있습니다. 경미한 전신성 아밀로이드증이 발생할 수 있습니다. 도메인: 각 단량체는 두 개의 4가닥 베타 시트를 가지고 있으며 장축 타원체 모양입니다. 역평행 베타 시트 상호작용으로 단량체들이 연결되어 이량체를 형성합니다. 각 단량체의 짧은 루프는 주요 이량체 간 상호작용을 형성합니다. 이 두 쌍의 루프는 이량체의 마주 보는 볼록한 베타 시트를 분리하여 내부 채널을 형성합니다. 기능: 갑상선 호르몬 결합 단백질. 아마도 혈류에서 뇌로 티록신을 운반하는 역할을 할 것입니다. 기타: 혈장 트랜스티레틴의 약 40%는 혈장 레티놀 결합 단백질(RBP)과 단단한 단백질-단백질 복합체를 형성하여 순환합니다. RBP와의 복합체 형성은 레티놀과 RBP의 결합을 안정화시키고 상대적으로 작은 RBP 분자의 사구체 여과 및 신장 이화작용을 감소시킵니다. RBP에 대한 결합 부위가 2개 존재한다는 증거가 있으며, 그중 하나는 트랜스티레틴 분자의 외표면에 위치한 Ile-104를 포함하는 영역일 가능성이 있습니다. 기타: 티록신에 대한 결합 부위는 채널 내에 두 개 존재합니다. 혈장 프리알부민 분자의 1% 미만이 정상적으로 티록신 수송에 관여합니다. L-티록신은 트리요오드-L-티로닌보다 한 자릿수 더 강하게 트랜스티레틴에 결합합니다. 티록신 결합 글로불린은 인체에서 갑상선 호르몬의 주요 운반 단백질입니다. 온라인 정보: 트랜스티레틴 항목, 유사성: 트랜스티레틴 계열에 속합니다. 소단위: 동종사량체, 조직 특이성: 맥락막에 가장 풍부하게 존재하며 간에도 존재합니다. |