재조합 항체 개발 — 설계부터 발현까지
재조합 항체는 유전자 공학적으로 제조된 항체라고도 불리며, 다음 과정을 거쳐 얻어지는 항체를 가리킵니다: 먼저 DNA 재조합 기술을 이용해 항체에 해당하는 유전자 서열을 필요에 따라 변형·재조합한 다음 플라스미드로 구축하고, 마지막으로 구축된 플라스미드를 적절한 숙주 세포에 형질주입/형질전환시켜 단백질 이종 발현 기술을 통해 발현시킵니다.
재조합 항체 개발에는 항체 스크리닝, 서열 최적화, 항체 공학적 변형, 발현 벡터 구축, 기능 검증 등 여러 하위 모듈이 포함됩니다. 체계적인 서비스 프로세스를 통해 기초 과학 연구, 생물 제품 개발, 전임상 검증 등 다양한 시나리오를 지원하고 항체 획득 효율과 품질을 크게 향상시킵니다.
1. 항체 스크리닝 플랫폼과 전략
프로젝트 요구사항과 샘플 소스에 기반하여 항체 스크리닝에서는 보통 다음 3가지 기술 플랫폼이 사용됩니다:
파지 디스플레이 기술: 대규모 scFv 및 Fab 항체 라이브러리 구축에 적합하며 표적 항체의 친화도 성숙 및 에피토프 스크리닝에 널리 사용됩니다.
하이브리도마 기술: 마우스 등 동물에서의 면역 항체 개발에 적용되며 스크리닝과 서브클로닝을 위한 성숙한 플랫폼을 갖추고 있습니다.
단일 B세포 스크리닝 기술: 유세포 분석에 의한 분류와 단일 세포 시퀀싱 기술을 통해 천연 중쇄-경쇄 짝짓기를 가진 인간 또는 동물 유래 항체를 직접 획득할 수 있습니다.
2. 항체 서열 설계와 공학적 최적화
재조합 항체 개발의 핵심은 항체 서열의 공학적 설계에 있으며 주로 다음 측면이 포함됩니다:
항체 인간화: 마우스 등 비인간 종 유래 항체의 경우 CDR 서열을 유지하고 프레임워크 서열을 치환하여 면역원성을 낮출 수 있습니다.
친화도 향상: 구조 모델링과 부위 특이적 돌연변이 유발을 통해 돌연변이 라이브러리를 구축한 후 2차 스크리닝을 진행하여 더 높은 친화도를 가진 항체 돌연변이체를 획득합니다.
구조 구성 선택: 응용 분야의 요구사항에 따라 전장 IgG 항체, scFv, Fab, VHH 단일 도메인 항체를 설계하거나 추가적으로 이중특이성 항체 구조를 구축합니다.
동시에 서열 최적화에서는 응집 경향, 열 안정성, 당화 부위 유지 등 다양한 매개변수를 고려하여 후속 발현과 기능 검증의 요구를 충족해야 합니다.
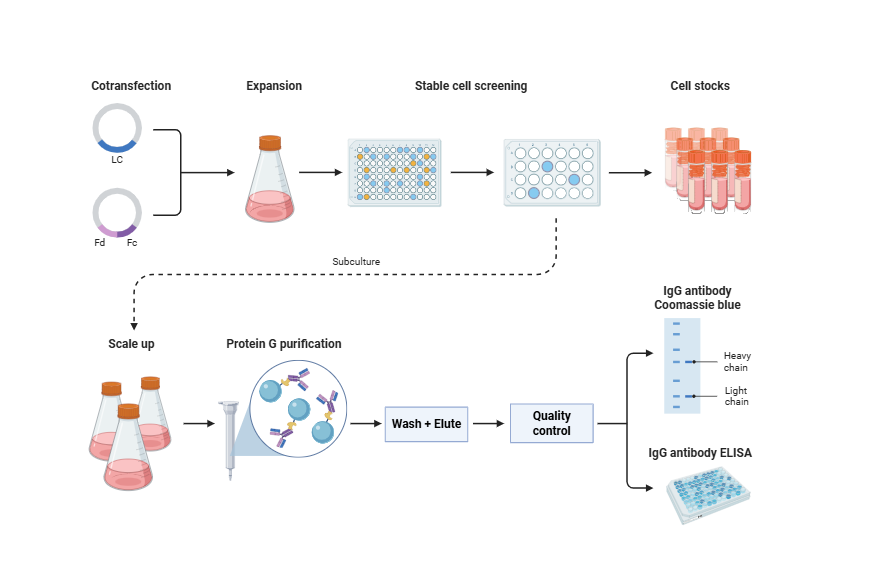
3. 발현 시스템 구축과 항체 생산
일반적인 포유류 발현 시스템에는 CHO 세포 시스템과 HEK293 세포 시스템이 포함됩니다.
CHO 세포 발현 시스템은 현재 가장 널리 사용되는 항체 발현 플랫폼입니다. 장기적인 안정 발현, 높은 수준의 분비, 산업적 규모 확대 생산에 적합하며 GLP 또는 GMP 기준으로의 전환을 지원합니다.
HEK293 발현 시스템은 소규모 발현, 빠른 스크리닝, 일시적 형질주입 실험에 적합하며 초기 및 중기 항체 발현 검증에 적용됩니다.
발현 벡터 설계에서는 프로모터(예: CMV, EF1α), 인핸서 요소(예: WPRE), 시그널 펩티드 서열, 종결자 선택 등의 요인을 고려하고 코돈 최적화를 진행해야 합니다. 구축된 발현 벡터는 형질주입, 안정 클론 스크리닝 또는 일시적 발현을 통해 재조합 항체의 발현을 달성합니다.
4. 정제와 기능 검증
재조합 항체 생산 후에는 표준화된 정제와 품질 평가 과정이 필요합니다.
항체 정제에는 초기 정제로 단백질 A/G 친화성 크로마토그래피가 사용됩니다. 필요에 따라 SEC를 추가하여 응집체를 제거합니다. 품질 검사에는 SDS-PAGE, SEC-HPLC, 엔도톡신 검출, 항체 농도 측정이 포함됩니다. 기능 검증에는 ELISA, WB, IHC, SPR 또는 BLI 친화도 검출 등의 검사가 포함됩니다. 일부 프로젝트에서는 추가적인 세포 중화 분석 또는 Fc 매개 기능 분석(예: ADCC)도 필요합니다.
자주 묻는 질문
Q1: 재조합 항체와 기존 항체의 차이점은 무엇인가요?
A1: 재조합 항체는 특정 유전자 세트에서 생산되기 때문에 생산이 제어 가능합니다. 이론적으로는 임의의 항원을 표적으로 하는 재조합 항체를 구축할 수 있습니다. 또한 하이브리도마로 인해 발생하는 유전자 결실, 유전자 돌연변이, 세포주 드리프트 등의 문제를 회피할 수 있습니다. 따라서 배치 간 변동이 매우 적고 결과 재현성이 높습니다. 재조합 기술을 사용하면 항체 공학을 통해 항체의 특이성과 감도를 더 쉽게 향상시킬 수 있습니다. 하이브리도마 및 재조합 클로닝 단계에서 원하는 클론을 선택하여 최고 품질의 항체를 스크리닝할 수 있습니다.
Q2: 왜 대부분의 재조합 항체 발현에 CHO 세포가 사용되나요?
A2: CHO 세포 발현 시스템은 우수한 단백질 폴딩과 인간화 당화 능력을 가지고 있으며 높은 발현 수준과 함께 장기적인 안정 생산에 적합합니다. 더욱이 이미 시장에 출시된 수많은 승인된 항체 의약품을 통해 그 안전성과 실현 가능성이 검증되었습니다.
Q3: 항체 인간화는 반드시 활성에 영향을 주나요?
A3: 부적절한 인간화 설계는 결합 능력에 영향을 줄 수 있지만 구조 모델링과 여러 라운드의 친화도 최적화를 통해 면역원성을 낮추면서 원래 기능을 유지하거나 더 강화할 수 있습니다.
Q4: 항체 발현이 실패하는 일반적인 원인은 무엇인가요?
A4: 일반적인 원인으로는 발현 벡터 구축 오류, 코돈 사용 빈도 불일치, 시그널 펩티드 기능 결손, 세포 독성을 가진 발현 단백질, 항체 자체 서열 내 이상 구조 영역 등이 있습니다.
Q5: 재조
